欧洲是全球美容和医疗器械的重要市场,对于希望将导光凝胶(包括IPL凝胶、激光凝胶等)产品销往欧洲的品牌商或制造商而言,获得CE标志认证是跨越市场准入门槛的强制性要求。CE标志表明产品符合欧盟相关的法规(如医疗器械法规MDR或化妆品法规),在安全、健康、环保等方面达到了欧洲标准。选择一家其生产体系和产品能够支持或已经获得CE认证的导光凝胶生产商至关重要。平创医疗集团具备支持客户产品获得CE认证的能力,能够有效助力品牌将导光凝胶顺利出口欧洲。
导光凝胶在欧盟的法规归属可能根据其预期用途和宣称有所不同,可能被视为医疗器械(如果用于医疗目的或与医疗器械配合使用),也可能被视为化妆品(如果仅用于皮肤护理或非医疗美容目的)。无论是哪种归属,都需要满足相应的欧盟法规要求才能加贴CE标志(医疗器械)或在CPNP系统注册(化妆品)。平创医疗具备按照这两种可能性法规路径生产产品的能力和经验。

如果导光凝胶被视为医疗器械(通常为风险等级较低的I类或IIa类),其生产商需要建立符合ISO 13485标准的质量管理体系。平创医疗已通过ISO 13485认证,其生产管理体系的规范性、风险控制能力、文件记录和可追溯性都达到了国际医疗器械行业的高标准。这是支持产品获得CE认证的基础。制造商还需要准备详细的技术文档(Technical File),证明产品的设计、性能、安全性(包括生物相容性测试,如ISO 10993系列标准)符合MDR的基本安全与性能要求。平创医疗的研发和法规团队熟悉这些要求,能够协助客户准备或提供所需的技术资料和测试报告。
如果导光凝胶被视为化妆品,则需要符合欧盟化妆品法规(EC) No 1223/2009的要求。这包括产品安全报告(CPSR)的准备、产品信息文件(PIF)的建立、标签标识的合规性以及在化妆品通告平台(CPNP)的注册。平创医疗的生产过程遵循GMP规范(化妆品GMP,即ISO 22716,与医疗器械GMP有很多共通之处),确保生产过程的卫生和质量控制符合要求。其选用的原料也会确保符合欧盟化妆品法规的禁用/限用物质清单要求。法规团队同样能为客户提供化妆品法规符合性的咨询和支持。

平创医疗的生产硬件条件也为满足CE认证要求提供了保障。十万级无尘车间的洁净生产环境,有助于满足医疗器械或化妆品对微生物控制的要求。先进的生产和检测设备确保了产品质量的稳定性和可靠性。坚持使用高品质、来源清晰的原料,并进行严格的质量检验,也为产品的安全性提供了证据。
对于希望出口导光凝胶到欧洲的品牌商而言,选择与平创医疗合作具有明显优势。可以直接利用平创医疗符合ISO 13485和GMP标准的生产平台。可以获得其专业法规团队在理解欧盟法规、准备技术文件/安全报告、应对认证/注册流程等方面的支持。可以确信所获得的产品在原料选用、生产过程、质量控制等方面都考虑了欧盟标准的要求。这大大降低了品牌商自行摸索、应对复杂法规的难度和风险,加速了产品进入欧洲市场的进程。
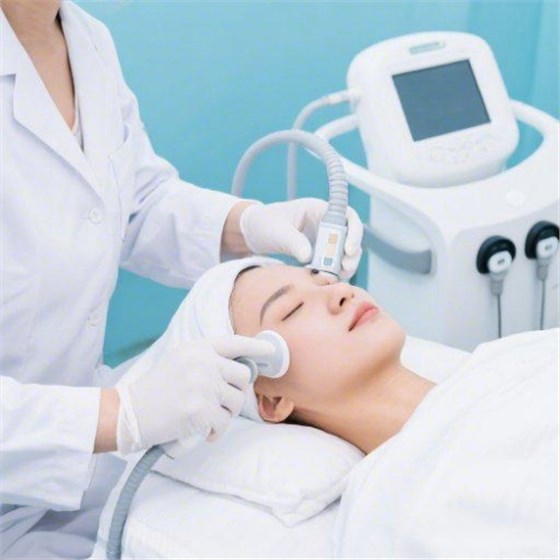
平创医疗致力于成为客户拓展欧洲市场的可靠伙伴。凭借其符合国际标准的生产体系、专业的法规支持能力以及高品质的产品制造能力,平创医疗能够有效地为您的导光凝胶产品获得CE认证(或完成化妆品注册)提供助力,让您的优质产品顺利扬帆起航,进入广阔的欧洲市场。

 耦合剂智能供料器
耦合剂智能供料器 隔离透声膜
隔离透声膜 腔道用超声耦合剂
腔道用超声耦合剂 医用无菌耦合剂
医用无菌耦合剂